Μαιευτική Γυναικολογική Μέριμνα
Αυτόματες Πρώιμες Και Κρυφές Αποβολές
Ακόμα και όταν οι συνθήκες είναι οι καλύτερες δυνατές, η μέγιστη
πιθανότητα κλινικά αναγνωρίσιμης εγκυμοσύνης είναι 30-40% σε κάθε
καταμήνιο (εμμηνορυσιακό) κύκλο .Υπάρχουν τεκμηριωμένες ενδείξεις ότι η
σχετικά χαμηλή γονιμότητα που παρατηρείται στο ανθρώπινο είδος οφείλεται
όχι στην αδυναμία σύλληψης αλλά στην προκλινική (πρώϊμη απώλεια ,
απώλεια τόσο νωρίς που είναι δύσκολο να αναγνωριστεί κλινικα) της
εγκυμοσύνης .Η συνεχής αύξηση του παγκόσμιου πληθυσμού φαίνεται να είναι
η απόδειξη για την γονιμότητα της ανθρώπινης φυλής . Ωστόσο , όταν η
ανθρώπινη αναπαραγωγή εξετάζεται από την άποψη της αποτελεσματικότητας ,
καθίσταται σαφές ότι η αύξηση του πληθυσμού έχει συμβεί για άλλους
λόγους , παρά ως αποτέλεσμα , της αναπαραγωγικής απόδοσής μας. Η σχετική
αναποτελεσματικότητα των ανθρώπων για την επίτευξη των ζώντων γεννήσεων
τονίστηκε με γραφικό τρόπο , όταν συγκρίθηκε ο αριθμός των εγγεγραμμένων
γεννήσεων στην Αγγλία το 1970 σε σύγκριση με τον αριθμό των αναμενόμενων
γεννήσεων όπως αυτός υπολογιζόταν βάσει των γόνιμων εμμηνορυσιακών
κύκλων για τον τότε αναπαραγωγικό πληθυσμό ( Roberts και Lowe , 1975 )
. Δεδομένου ότι μόνο το 22% των γόνιμων κύκλων που εκτέθηκαν σε
«κίνδυνο» ενδεχόμενης εγκυμοσύνης είχε ως αποτέλεσμα ζώντες γεννήσεις (
Πίνακας Ι ), οι συγγραφείς έθεσαν το ερώτημα «Πού πήγαν όλες οι
συλλήψεις ; "
| Μελέτη | Ομάδα Ελέγχου Μη Εγκύων | Τρόπος Υπολογισμού Ωορρηξίας | Κύκλοι Παρακολούθησης | Αποβολές |
| Chartier. 1979 | 12 | Με μέτρηση μέσης θερμοκρασίας | 321 | 49 [15%] |
| Miller 1980 | καμμία | Στην Μέση Του Κύκλου | 623 | 50 [8%] |
| Edmonds. 1982 | 50 με απολίνωση σαλπίγγων | Στην Μέση Του Κύκλου | 198 | 67 [34%] |
| Whittiker 1983 | καμμία | Στην Μέση Του Κύκλου | 226 | 7 [3%] |
Από τον παραπάνω πίνακα : Για την μελέτη του Edmonds για παράδειγμα , φάινεται ότι σε 198 κύκλους , μόνο το 51% είχε τελικά καθυστέρηση . Στο 34% ανιχνεύθηκε χοριακή χωρίς καθυστέρηση , και στο υπόλοιπο 15% δεν έγινε σύλληψη . Από όλες τις μελέτες βγαίνει συνολικά το ποσοστό των κρυφών αποβολών. Πιο πρόσφατες μελέτες έχουν δείξει ότι ακόμα και όταν οι συνθήκες για τη σύλληψη θεωρούνται οι καλύτερες δυνατές , η μέγιστη πιθανότητα αναγνωρίσιμης σύλληψης σε ένα κύκλο είναι περίπου 30 % ( Zinamen et ah , 1996 . Slama et al , 2002 ) . Το ποσοστό αυτό ανήλθε στο 40 % σε νεαρές γυναίκες που υποβλήθηκαν σε χρονομετρημένη γονιμοποίηση (σπερματέγχυση) με σπέρμα από δότες με αποδεδειγμένη γονιμότητα ( van Noord - Zaadstra et al , 1991 ) .
Τίθεται λοιπόν το ερώτημα πώς «εξαφανίζεται» ένα ποσοστό κυήσεων .
Η εγκυμοσύνη μπορεί να χαθεί ανά πάσα στιγμή μεταξύ γονιμοποίησης και
εμφύτευσης , ή ακόμη και αργότερα . Μόνον ένα μέρος αυτών των απωλειών
αποκαλύπτεται κλινικά ως αποβολές . Ωστόσο , δεδομένου ότι η πρώτη
έκθεση της απώλειας της εγκυμοσύνης ανιχνεύεται από τη μέτρηση της hCG (
Morris και Udry , 1967 ) , έχει καταστεί σαφές ότι ένας μεγάλος αριθμός
των συλλήψεων αποτυγχάνει πριν η γυναίκα αντιληφθεί ότι είναι έγκυος ,
πρίν ακόμα και από την πρώτη ημέρα καθυστέρησης . Αλλωστε , δεν κάνουν
όλες οι γυναίκες τέστ κυήσεως αίματος με μία μόνο μέρα καθυστέρησης .
Η εισαγωγή των ευαίσθητων δοκιμασιών αίματος για την μέτρηση της
χοριακής γοναδοτροφίνης (hCG) και η δυνατότητα που παρέχεται από την
εξωσωματική γονιμοποίηση για να παρατηρήσουμε τα γεγονότα από την
ωορρηξία ώς την εμφύτευση του εμβρύου , επέτρεψε την διερεύνηση της
προηγουμένως φευγαλέας και «απόκρυφης» ανάπτυξης της πρώϊμης εγκυμοσύνης
. Ουσιαστικά , μπορέσαμε να ανοίξουμε το «μαύρο κουτί» των γεγονότων
αυτών . Επίσης με τις νέες τεχνικές στην κυτταρογενετική, έχει αυξηθεί
η κατανόηση των φυσικών ορίων της ανθρώπινης γονιμότητας, με σαφείς
επιπτώσεις για τα όρια της επιτυχίας της εξωσωματικής γονιμοποίησης .
Η Χοριακή Γοναδοτροπίνη (hCG) Ως Δείκτης Για Πρώϊμη Αποβολή
Ο περισσότερο χρησιμοποιημένος δείκτης εγκυμοσύνης είναι η χοριακή
γοναδοτροφίνη . Σε αυτόν τον δείκτη έχουν βασιστεί όλες οι μελέτες που
αφορούν στην πρώϊμη απώλεια της εγκυμοσύνης . In-vitro μελέτες έχουν
δείξει ότι η hCG παράγεται από τροφοβλαστικά κύτταρα της βλαστοκύστης
και μπορεί να ανιχνευθεί από την 7η μέρα μετά τη γονιμοποίηση και μετά (Shutt
and Lopata, 1981; Fishel et al., 1984; Lachlan and Lopata, 1988; Lopata
and Hay, 1989).
Ωστόσο, η hCG που παράγεται από ένα κύημα θεωρείται γενικά ανιχνεύσιμη
στον μητρικό ορό ή τα ούρα μόνο από τη στιγμή της εμφύτευσης και μετά .
Στην πράξη, αυτό σημαίνει ότι γίνεται ανιχνεύσιμη 6,5-9,5 ημέρες μετά
την απότομη αύξηση της LH , μετά δηλαδή από την ωορρηξία . (Hay et al,
1986 Lenton και Woodward, 1988). Οι περισσότερες μετρήσεις χοριακής
αίματος γίνονται 14 ημέρες μετά την εμβρυομεταφορά για να συμπίπτουν με
την αναμενόμενη πρώτη ημέρα καθυστέρησης .
Η σταθερότητα της hCG την καθιστά κατάλληλη για τη μελέτη, δεδομένου
ότι, ιδίως στην αρχή της εγκυμοσύνης, οι μετρήσεις στα ούρα είναι
ακριβείς και αντιπροσωπεύουν σταθερά τις μετρήσεις στον ορό (Wehmann
1981. Norman 1987.). Επιπλέον, η hCG είναι πολύ σταθερή , ακόμη και στα
ούρα τα οποία έχουν επανειλημμένα καταψυχθεί και αποψυχθεί (McCready
1978 , Wilcox 1985). Η ανάπτυξη αντισωμάτων έναντι της β-υπομονάδας της
hCG ήταν μια βελτίωση σε σχέση με προηγούμενες δοκιμασίες (Vaitukaitis
1972), αλλά η ανάπτυξη των ανοσοραδιομετρικών δοκιμασιών τελικά παρείχε
μια πολύ ευαίσθητη και ειδική μέθοδο μέτρησης της χοριακής στον ορό και
στα ούρα (Wilcox 1985 Canfield 1987).
Υπάρχουν πάρα πολλές μελέτες που χρησιμοποίησαν την χοριακή ως δείκτη
για τον εντοπισμό πολύ πρώιμων αποβολών : Wilcox 1999 , Stewart 1993 ,
Lenton 1991, Liu 1991 , Stewart 1993 , Hearn 1991 , Rogers 1995 .
Οταν λαμβάνονται μαζί, τα δεδομένα από τις δημοσιευμένες μελέτες
δείχνουν ένα ρυθμό απώλειας εγκυμοσύνης πριν την εμφύτευση της τάξεως
του 30%, ένα επιπλέον 30% μετά την εμφύτευση αλλά πριν από την χαμένη
περίοδο, και 10% ως αναγνωρισμένες κλινικά αποβολές (Σχήμα 1). Το
συμπέρασμα είναι ότι 60% των συλλήψεων δεν προχωρούν . Και αυτό δεν
δηλώνει παθολογία . Απλά συμβαίνει . Το γεγονός αυτό αντικατοπτρίζεται
στην σύγχρονη πρακτική της διερεύνησης της υπογονιμότητας . Πράγματι ,
ένα ζεύγος πρέπει να έχει ένα διαστημα ενός έτους ελεύθερων επαφών χωρίς
επιτυχία για να χαρακτηριστεί υπογόνιμο .
(δείτε επίσης Διάστημα Ελεύθερων Επαφών)
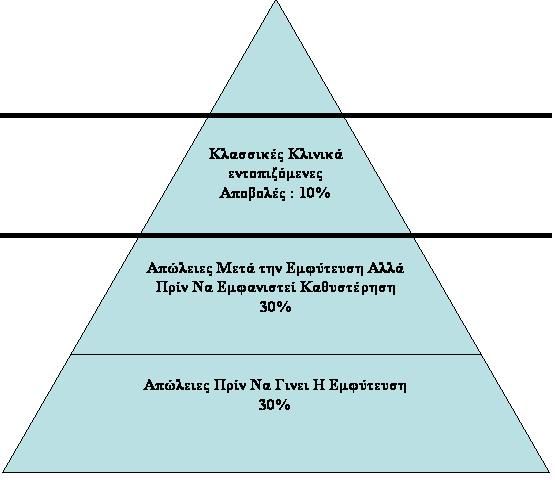
Πυραμίδα Πρώϊμων Αποβολών.
Το "παγόβουνο" των πρώϊμων αποβολών . Μια επισκόπηση των αποτελεσμάτων της αυθόρμητης ανθρώπινης εγκυμοσύνης (spontaneous human pregnancy)
Κλασσικές Κλινικά εντοπιζόμενες Αποβολές 10% , Απώλειες Μετά την Εμφύτευση Αλλά Πρίν Να Εμφανιστεί Καθυστέρηση 30% , Απώλειες Πρίν Να Γινει Η Εμφύτευση 30%.
Συνολικά το 70% των συλλήψεων χάνονται πριν να προχωρήσει η εγκυμοσύνη . Η πλειονότητα αυτών των απωλειών (60%) συμβαίνουν πριν από το χρόνο της χαμένης εμμηνορροϊκής περιόδου , δηλαδή πρίν την πρώτη μέρα καθυστέρησης , και έτσι δεν αποκαλύπτονται. (Προσαρμογή από Chard, 1991.) Ενώ μελέτες όπως οι παραπάνω μας έχουν βοηθήσει στην κατανόηση των κρυφών αποβολών , η τύχη του γονιμοποιημένου ωαρίου πριν από την εμφύτευση παραμένει ασαφής . Η εμφύτευση ξεκινά γύρω στην 8η ημέρα μετά την απότομη αύξηση της LH ( 82 , Enders και Lopata 1999 ) . Μολονότι υπάρχουν ευαίσθητες δοκιμασίες ικανές να ανιχνεύσουν αυξήσεις στην hCG που παράγεται από το έμβρυο πριν από την εμφύτευση ( Chang 1998 ) οι in - vivo μελέτες του προεμφυτευτικού εμβρύου (δηλαδή η μελέτη του εμβρύου πρίν την εμφύτευση σε σημείο που βρίσκεται κάπου στην σάλπιγγα) απαιτούν έναν δείκτη που καθίσταται ανιχνεύσιμος από τη στιγμή της γονιμοποίησης και μετά. Μια πολλά υποσχόμενη υποψήφια ουσία είναι ο « παράγοντας εγκυμοσύνης » (pregnancy factor) ο οποίος εκκρίνεται εντός του μητρικού ορού 12 – 16 ώρες μετά τη γονιμοποίηση. Αυτή η εντοπίστηκε για πρώτη φορά το 1977 ( Morton 1977 . ) Και στη συνέχεια βρέθηκε να εκκρίνεται από προεμφυτευτικά έμβρυα ( Bose , 1989 , 1991 ) . Η παρουσία του παράγοντα εγκυμοσύνης στο μέσο καλλιέργειας των ζυγωτών και η απουσία του από μη γονιμοποιημένα ωοκύτταρα υποδεικνύουν ότι είναι ένα προϊόν του αναπτυσσόμενου εμβρύου ( Daya and Clark , 1986 , 1988 ) . Πιο πρόσφατες μελέτες έχουν επικεντρωθεί στην ευαισθησία και την ειδικότητα του pregnancy factor ανίχνευση σύλληψης in νίνο ( Fan και Zheng , 1997 ) πρίν από τη χοριακή . Αλλά μέχρι τώρα η χρησιμότητα αυτού του δείκτη δεν έχει ακόμη τεκμηριωθεί και η χοριακή παραμένει ο καλύτερος και πρωϊμότερος δείκτης εγκυμοσύνης .
Γενετικοί Παράγοντες
Είναι σαφές ότι οι μελέτες που χρησιμοποιούν δείκτες για τη σύλληψη, την εμφύτευση και την κύηση σε εξέλιξη μπορούν να παρέχουν μόνο περιορισμένες πληροφορίες σχετικά με την τύχη του μετά τη γονιμοποίηση ωαρίου , δηλαδή του ζυγωτού . Μεγάλο μέρος της προόδου για τη βελτίωση της κατανόησης των γεγονότων της πολύ πρώιμης κύησης έχει γίνει στον τομέα της κυτταρογενετικής. Η πιθανή σημασία των γενετικών ανωμαλιών ως οι πιθανές αιτίες της πρόωρης απώλειας της εγκυμοσύνης κατέστη σαφής από τις μελέτες των αυτόματων αποβολών . Οι χρωμοσωμικές ανωμαλίες προέκυψαν στο > 50 % των αποβληθέντων κυήσεων ( Boue et 1975 Eiben 1987 . ) . Από τις αρχές της δεκαετίας του ογδόντα έχει μελετηθεί και η συχνότητα των χρωμοσωμικών ανωμαλιών σε ωοκύτταρα , ζυγώτες και τα πρώτα στάδια της ανάπτυξης του εμβρύου. Λόγω νομικών περιορισμών στις περισσότερες χώρες , τα ανθρώπινα έμβρυα για τη μελέτη προήλθαν από το εσωτερικό πλαίσιο της θεραπείας της υπογονιμότητας και συνεπώς δεν αντικατοπτρίζουν την κανονική κατάσταση . Ωστόσο , έχει καταστεί δυνατό να μελετηθούν κανονικά ωοκύτταρα από ζευγάρια με υπογονιμότητα ανδρικού παράγοντα και αντιστρόφως , καθώς και την μελέτη με την εισαγωγή νέων μεθόδων κυτταρογενετικής . Οι διάφοροι τύποι του φθορισμού in situ υβριδισμού ( FISH ) που είναι τώρα διαθέσιμες έχουν οδηγήσει σε αξιόπιστες εκτιμήσεις της ανευπλοειδίας σε επιμέρους βλαστομερή , και την συμβολή του χρωμοσωμικού μωσαϊκισμού στην πρώιμη εμβρυϊκή απώλεια .
Ανευπλοειδίες σε ωοκύτταρα
Από την πρώτη έκθεση σχετικά με τη μελέτη της μειωτικής διαίρεσης στα ανθρώπινα ωοκύτταρα το 1968, ένας μεγάλος αριθμός των δημοσιεύσεων περιέγραψε την κυτταρογενετική ανάλυση των ωαρίων απέτυχαν να γονιμοποιήθουν από τα προγραμματα εξωσωματικής γονιμοποίησης . Μια αύξηση στην ηλικία της μητέρας οδηγεί σε αυξημένο συντελεστή εμβρυϊκής ανευπλοειδίας , καθώς και την αυξημένη συχνότητα των αυτόματων αποβολών . Και οι δύο αυξήσεις προκύπτουν από τον μή αποχωρισμό των χρωμοσωμάτων προκαλώντας αυτοσωματική τρισωμία ( Hook , 1981 ) . Για όλα τα χρωμοσώματα , εκτός από το μεγαλύτερο , ο μή αποχωρισμός των χρωμοσωμάτων αυξάνει σε συχνότητα με την ηλικία . Από την άλλη πλευρά , η μονοσωμία Χ δείχνει ένα αντίστροφο συσχετισμό με την ηλικία της μητέρας . Γενικά , τα ευρήματα από τις κυτταρογενετικές μελέτες επιβεβαιώνουν την υπόθεση ότι τα ωοκύτταρα των ηλικιωμένων γυναικών είναι πιο επιρρεπη σε μη αποχωρισμό των χρωμοσωμάτων που προκαλείται από σφάλματα στην μειωτική διαίρεση στο επίπεδο των γαμετών (ωάρια για τη γυναίκα , σπέρματοζωάρια για τον άνδρα) . Ωστόσο , η επίδραση της ηλικίας της μητέρας για την εμβρυϊκή ανευπλοειδία , είναι καλά τεκμηριωμένη . Επίσης οι ενδο-και εξωθυλακιωτικές (extrafollicular) επιρροές ( περιθυλακική μικροαγγείωση , ελλειπής οξυγόνωση , η παρουσία των καταλοίπων από τον καπνό του τσιγάρου κλπ. ) είναι σε θέση να διαταράξουν την ωρίμανση και να οδηγήσουν σε ανευπλοειδία . Η Μειωτική διαδικασία των ωοκυττάρων είναι πολύ ευαίσθητη στους ενδογενείς ή / και στους εξωγενείς παράγοντες ( Plachot , 1997 ) .
Ανωμαλίες στις κλινικά αναγνωρισμένες αποβολές
Η μελέτη των χρωμοσωμικών ανωμαλιών στα δείγματα από αποβολές είναι δύσκολο να πραγματοποιηθεί . Συχνά το υλικό δεν είναι κατάλληλο για κυτταρογενετικό παρασκεύασμα , ιδιαίτερα όταν η αποβολή είναι καθυστερημένη και το υλικό έχει τύχει επεξεργασίας από μητρικά φαγοκύτταρα . Επίσης , μπορεί κατά λάθος να μπεί σε φορμόλη , οπότε ο καρυότυπος είναι αδύνατος . Μερικά δείγματα δεν δείχνουν καμία ανάπτυξη, διότι ο ενδομήτριος θάνατος επήλθε πολύ πριν εξαχθεί ο ιστός με απόξεση . Τέλος υπάρχει και το οικονομικό κόστος . Ως εκ τούτου, οι κυτταρογενετικές μελέτες σε υλικό αποβολής είναι επιτυχείς μόνο σε λίγες περιπτώσεις , εκτός και άν αυτό γίνει προγραμματισμένα .
Η πρώϊμη "αποβολή" και η υπογονιμότητα
Τα ερωτήματα για το κατά πόσον ή όχι
Α) Αν η πρόωρη – κρυφή - απώλεια της εγκυμοσύνης μπορεί να εκδηλωθεί ως
στειρότητα σε ζευγάρια που προσπαθούν να συλλάβουν,
ή
Β) Αν τα υπογόνιμα ζευγάρια είναι πιο επιρρεπή σε πρόωρη ή και κρυφή
απώλεια εγκυμοσύνης
παραμένουν θέματα συζήτησης κυρίως λόγω αδυναμιών στατιστικής
ποσόστωσης των περιπτώσεων .
Επιπλέον, ο φαινομενικά υξημένος κίνδυνος αποβολών που αναφέρται σε
υπογόνιμες γυναίκες μπορεί να οφείλεται σε προκατάληψη ανίχνευσης
δεδομένου ότι οι γυναίκες αυτές κάνουν τεστ εγκυμοσύνης νωρίτερα, και
συνεπώς, αναγνωρίζουν περισσότερες αποβολές (Baird 1993) . Αν και οι
γυναίκες που δεν προσπαθούν να συλλάβουν ελέγχονται με χοριακή αίματος ή
ούρων στην 1η μέρα καθυστέρησης είναι αρκετά πιθανό να ανέκυπταν
παρόμοια στατιστικά στοιχεία . Παρά τις πιθανότητες για υπερ-εκπροσώπηση
των πρόωρων αποβολών στον υπογόνιμο πληθυσμό, μια σειρά από μελέτες ΔΕΝ
έχουν δείξει καμία τέτοια συσχέτιση (Sharp 1986, Liu 1988, Wilcox
1988).
Εκείνο που γνωρίζουμε όμως είναι ότι ένα απόλυτα φυσιολογικό ζευγάρι
έχει 20-30-40% πιθανότητες να συλλάβει σε κάθε κύκλο . Πρέπει να
συνειδητοποιήσουμε , ότι ενώ θα θέλαμε να είμαστε 100% επιτυχείς (ένας
καταμήνιος κύκλος = μία γέννηση!) , στην πραγματικότητα δεν είμαστε .
Και όχι σαν άτομα . Αλλά σαν είδος .
Επίσης μάλλον θα έπρεπε να είμαστε ευγνώμονες για το 60% των συλλήψεων
που δεν αντιλαμβανόμαστε . Είναι η φυσική επιλογή που ουσιαστικά
δουλεύει για το ζεύγος προσπαθώντας να προσφέρει ένα υγιές παιδί , έστω
και δυο-τρείς μήνες αργότερα ! Αν άλλωστε , οι χρωμοσωμικά ανώμαλες
κυήσεις αυτές προχωρούσαν (πέραν των 2-3 ημερών βιολογικής ζωής του
γονιμοποιημένου ωαρίου όπως συμβαίνει τώρα) η γυναίκα θα σπαταλούσε χρόνο
από την συνολική χρονική διάρκεια της γονιμότητάς της κυοφορώντας ένα
έμβρυο που π.χ θα αποβληθεί στην 25 εβδομάδα , χάνοντας έτσι 6-7 κύκλους
! Η φύση ίσως τελικά να μήν είναι τόσο σκληρή όσο νομίζουμε .
Ορισμοί
Οι ορισμοί διαφέρουν λίγο από την αγγλική ορολογία , διότι η γονιμότητα
στα ελληνικά εμπεριέχει μέσα της την έννοια της επιτυχούς έκβασης της
εγκυμοσύνης δηλαδή της γέννησης .
Μηνιαία Πιθανότητα Σύλληψης Κύκλου
είναι η πιθανότητα εγκυμοσύνης στο διάστημα ενός έμμηνου κύκλου επαφών .
Fecundability is the probability of being pregnant in a single menstrual
cycle
Κύκλος γονιμότητας
είναι η πιθανότητα για ένα κύκλο να οδηγήσει σε ζών νεογνό. Fecundity
is the probability of achieving a live birth within a single cycle
Κλινικά αποδεδειγμένη κύηση
= θετική χοριακή , σάκος κύησης , έμβρυο , καρδιακή λειτουργία ,
καθυστέρηση .
Κρυφή , ή Πολύ Πρώιμη Αποβολή
α) Η απώλεια γονιμοποιημένου ωαρίου που δεν προκαλεί καθυστέρηση , με
μή ανιχνεύσιμη χοριακή
β) Η απώλεια γονιμοποιημένου ωαρίου που δεν προκαλεί καθυστέρηση με
ελάχιστα επίπεδα χοριακής (κάτω από 5)
β) Η απώλεια γονιμοποιημένου ωαρίου που προκαλεί μικρή καθυστέρηση στα
πλαίσια του χρονικού εύρους του κύκλου αλλά με ελάχιστη , μή ανιχνεύσιμη
χοριακή .
γ) Η απώλεια γονιμοποιημένου ωαρίου που ενώ υπάρχει ζυγωτό , δεν
προκαλεί ούτε καθυστέρηση ούτε αύξηση χοριακής
Προσέξτε ότι ο όρος «αποβολή» χρησιμοποιείται σχεδόν καταχρηστικά .
Προτιμάται ο όρος «απώλεια ζυγωτού» ή απώλεια «γονιμοποιημένου ωαρίου» .
ΟΙ "ΑΠΟΒΟΛΕΣ" ΑΥΤΟΥ ΤΟΥ ΕΙΔΟΥΣ ΔΕΝ ΣΥΜΠΕΡΙΛΑΜΒΑΝΟΝΤΑΙ ΣΤΗ ΝΟΣΟΛΟΓΙΚΗ
ΟΝΤΟΤΗΤΑ ΤΩΝ ΚΑΘ'ΕΞΙΝ ΑΠΟΒΟΛΩΝ .
Ερωτήσεις - Απαντήσεις [back to top]
Βιβλιογραφία
Adinolfi, M., Pertl, B. and Sherlock, J. (1997) Rapid detection of aneuploidies
by microsatellite and the quantitative fluorescent polymerase chain reaction.
Prenat. Diagn., 17, 1299-1311.
Angell, R.R. (1991) Predivision in human oocytes at meiosis I: a mechanism for
trisomy formation in man. Hum. Genet., 86, 383-387.
Angell, R.R. (1994) Cytogenetic analysis of unfertilized human oocytes. In
Mastroianni, L. Jr, Coeling Bennink, H.J.T., Suzuki, S. and Vemer, H.M. (eds)
Gamete and Embryo Quality. Parthenon, London, UK, pp. 47-62.
Angell, R.R. (1997) First-meiotic division nondisjunction in human oocytes. Am.
J. Hum. Genet., 61, 23-32.
Baird, D.D., Wilcox, A.J. and Weinberg, C.R. (1986) Use of time to pregnancy to
study environmental exposures. Am. J. Epidemiol., 124, 470-480.
Baird, D.D., Ragan, N.B. and Wilcox, A.J. (1993) The relationship between
reduced fecundability and subsequent fetal loss. In Gray, R. (ed.) Biochemical
and Demographic Determinants of Reproduction. Clarendon Press, Oxford, UK.
Benkhalifa, M., Janny, L., Vye, P., Malet, P., Boucher, D. and Menezo, Y.
(1993) Αssessment of polyploidy in human morulae and blastocysts using
co-culture and fluorescent in-situ hybridization. Hum. Reprod., 8, 895- 902.
Bergh, P.A. and Navot, D. (1992) The impact of embryonic development and
endometrial maturity on the timing of implantation. Fertil. Steril., 58,
537-542.
Bielanska, M., Tan, S.L. and Ao, O. (2000) Significance of mosaicism in the
human preimplantation embryo. Hum. Reprod., 15 (Abstract Book), 12. Bjercke, S.,
Tanbo, T.,
Dale, P.O., M0rkrid, L. and Abyholm, T. (1999) Human chorionic gonadotrophin
concentrations in early pregnancy after in-vitro fertilization. Hum. Reprod.,
14, 1642-1646.
Bloch, S.K. (1976) Occult pregnancy: a pilot study. Obstet. Gynecol., 48, 365-
368.
Bonduelle, M.L., Dodd, R., Liebaers, I., Van Steirteghem, Α., Williamson, R.
and Akhurst, R. (1988) Chorionic gonadotrophin-beta mRNA, a trophoblast marker,
is expressed in human 8-cell embryos derived from tripronucleate zygotes. Hum.
Reprod., 3, 909-914.
Βongso, Α., Ng, S.C., Lim, J., Fong, C.Y. and Ratnam, S. (1991) Preimplantation
genetics: chromosomes of fragmented human embryos. Fertil. Steril., 56, 66-70.
Bose, R. (1989) Human embryo associated immunosuppressor factor(s) from pre- and
post-implantation stages share some similarities. Immunol. Lett., 20, 261-268.
Bose, R. (1991) The partially purified pre-implantation suppressor factor may
be one of several factors to play a role in successful pregnancy. Immunol. Lett.,
27, 119-126.
Bose, R., Cheng, H., Sabbadini, E., McCoshen, J., Mahadevan, M.M. and Fleetham,
J. (1989) Purified human early pregnancy factor from preimplantation embryo
possesses immunosuppressive properties. Am. J. Obstet. Gynecol., 160, 954-960.
Boue, J., Boue, A. and Lazar, P. (1975) Retrospective and prospective
epidemiological studies of 1500 karyotyped spontaneous human abortions.
Teratology, 12, 11-26.
Buster, J.E., Bustillo, M., Rodi, I.A., Cohen, R.N.P, Hamilton, M., Simon,
J.A., Thorneycroft, I.H. and Marshall, J.R. (1985) Biologic and morphologic
development of donated human ova recovered by nonsurgical uterine lavage. Am. J.
Obstet. Gynecol., 153, 211-217.
Canfield, R.E., O'Connor, J.F., Birken, S., Krivechy, A. and Wilcox, A.J. (1987)
Development of an assay for a biomarker of pregnancy and early fetal loss.
Environ. Health. Perspect., 74, 57-66.
Carr, D.H. (1963) Chromosome studies in abortuses and stillborn infants.
Lancet, ii, 603-606.
Cavanagh, A.C. (1996) Identification of early pregnancy factor as chaperonin
10: implications for understanding its role. Rev. Reprod., 1, 28-32.
Chang, P.L., Canfield, R.E., Ditkoff, E.C., O'Connor, J.F. and Sauer, M.V.
(1998) Measuring human chorionic gonadotropin in the absence of implantation
with use of highly sensitive urinary assays for intact beta- core and free beta
epitopes. Fertil. Steril., 69, 412—414.
Chard, T. (1991) Frequency of implantation and early pregnancy loss in natural
cycles. Baill. Clin. Obstet. Gynaecol., 5, 179-189.
Chartier, M., Roger, M., Barrat, J. and Michelon, B. (1979) Measurement of
plasma chorionic gonadotropin (hCG) and β-hCG activities in the late luteal
phase: evidence of the occurrence of spontaneous menstrual abortions in
infertile women. Fertil. Steril., 31, 134-137.
Coonen, E., Harper, J.C., Ramaekers, F.C., Delhanty, J.D., Hopman, A.H.,
Geraedts, J.P. and Handyside, A.H. (1994) Presence of chromosomal mosaicism in
abnormal preimplantation embryos detected by fluorescence in situ hybridisation.
Hum. Genet., 94, 609-615.
Dailey, T., Dale, B., Cohen, J. and Munne, S. (1996) Association between
nondisjunction and maternal age in meiosis-II human oocytes. Am. J. Hum. Genet.,
59, 176-184.
Daya, S. and Clark, D.A. (1986) Production of immunosuppressor factor(s) by
preimplantation embryos. Am. J. Reprod. Immunol. Microbiol., 11, 98- 101.
Daya, S. and Clark, D.A. (1988) Identification of two species of suppressive
factor of different weight released by in vitro fertilized human oocytes. Fertil.
Steril., 49, 360-363.
Delhanty, J.D., Harper, J.C., Ao, Α., Handyside, A.H. and Winston, R.M. (1997)
Multicolour FISH detects frequent chromosomal mosaicism and chaotic division in
normal preimplantation embryos from fertile patients. Hum. Genet., 99, 755-760.
Durban, M., Benet, J., Sarquella, J., Egozcue, J. and Navarro, J. (1998)
Chromosome studies in first polar bodies from hamster and human oocytes. Hum.
Reprod., 13, 583-587.
Edmonds, D.K., Lindsay K.S., Miller, J.F., Williamson, E. and Wood, P.J. (1982)
Early embryonic mortality in women. Fertil. Steril., 38, 447^1-53.
Eiben, B., Borgmann, S., Schuebbe, I. and Hansmann, I. (1987) A cytogenetic
study directly from chorionic villi of 140 spontaneous abortions. Hum. Genet.,
11, 137-141.
Enders, A.C. and Lopata, A. (1999) Implantation in the marmoset monkey:
expansion of the early implantation site. Anat. Rec., 256, 279-299.
Evsikov, S. and Verlinsky, Y. (1998) Mosaicism in the inner cell mass of human
blastocycts. Hum. Reprod., 13, 3151-3155.
Fan, X.G. and Zheng, Z.Q. (1997) A study of early pregnancy factor activity in
preimplantation. Am. J. Reprod. Immunol., 37, 359-364.
Findlay, I., Toth, T., Matthews, P. Marton, T., Quirke, P. and Papp, Z. (1998)
Rapid trisomy diagnosis (21, 18 and 13) using fluorescent PCR and short tandem
repeats: applications for prenatal diagnosis and preimplantation genetic
diagnosis. J. Ass. Reprod. Genet., 15, 266-275.
Fishel, S.B., Edwards, R.G. and Evans, C.J. (1984) Human chorionic gonadotropin
secreted by preimplantation embryos cultured in vitro. Science, 223, 816-818.
Formigli, L., Formigli, G. and Roccio, C. (1987) Donation of fertilized uterine
ova to infertile women. Fertil. Steril., 47, 162-165.
Fritz, B., Hallermann, C., Olert, J., Fuchs, B., Bruns, M., Asian, M., Schmidt,
S., Coerdt, W., Muntefering, H. and Rehder, H. (2001) Cytogenetic analyses of
culture failures by comparative genomic hybridisation (CGH)—Re-evaluation of
chromosome aberration rates in early spontaneous abortions. Eur. J. Hum. Genet.,
9, 539-547.
Fung, J., Hyun, W., Dandekar, P. Pedersen, R. and Weier, H. (1998) Spectral
imaging in preconception/preimplantation genetic diagnosis of aneuploidy:
multicolor, multichrome screening of single cells. J. Ass. Reprod. Genet., 15,
323-330.
Gardner, D.K., Lane, M., Stevens, J. and Schoolcraft, W.B. (2001) Noninvasive
assessment of human embryo nutrient consumption as a measure of developmental
potential. Fertil. Steril., 76, 1175-1180.
Gianaroli, L., Magli, M.C., Ferraretti, A.P., Fortini, D., Tabanelli, C. and
Gergolet, M. (2000) Gonadal activity and chromosomal constitution of in vitro
generated embryos. Mol. Cell. Endocrinol., 30, 111-116.
Guerneri, S., Bettio, D., Simoni, G., Brambati, B., Lanzani, A. and Fraccaro, M.
(1987) Prevalence and distribution of chromosome abnormalities in a sample of
first trimester internal abortions. Hum. Reprod., 2, 735-739.
Pieters, M.H.E.C., Dumoulin, Ignoul-Vanvuchelen, R.C.M., Bras, M.,
Evers, J.L.H. and Geraedts, J.P.M. (1992) Triploidy after in vitro
fertilization: cytogenetic analysis of human zygotes and embryos. J. Assist.
Reprod. Fertil., 9, 68-76.
Plachot, M. (1997) The human oocyte. Genetic aspects. Ann. Genet., 40, 115— 120.
Plachot, M. (2001) Chromosomal abnormalities in oocytes. Mol. Cell. Endocrinol.,
183, S59-S63.
Plachot, M., Grouchy de, J., Junca, A.M., Mandelbaum, J., Turleau, C., Couillin,
P., Cohen, J. and Salat-Baroux, J. (1988) From oocyte to embryo: A model,
deduced from in vitro fertilization, for natural selection against chromosome
abnormalities. Annales de Genetique, 30, 22-32.
Plachot, M., Mandelbaum, J., Junca, A.M., de Grouchy, J., Salat-Baroux, J. and
Cohen, J. (1989) Cytogenetic analysis and developmental capacity of normal and
abnormal embryos after IVF. Hum. Reprod., 4 (Suppl.), 99- 103.
Roberts, J. and Lowe, R. (1975) Where have all the conceptions gone? Lancet, i,
498-500.
Rogers, P.A.W. (1995) Current studies on human implantation: a brief overview.
Reprod. Fertil. Dev., 1, 1395-1397.
Ruangvutilert, P. Delhanty, J. Serhal, P. Simopoulou, M. Rodeck, C. and Harper,
J. (2000) Fish analysis on day 5 post-insemination of human arrested and
blastocyst stage embryos. Pren. Diagn., 20, 552-560.
Sandalinas, M., Sadowy, S., Calderon, G., Escudero, T., Alikani, M., Cohen, J.
and Munne, S. (2000) Survival of chromosome abnormalities to blastocyst stage.
Hum. Reprod., 15 (Abstract book), 11.
SART/ASRM (2002) Assisted reproductive technology in the United States: 1998
results generated from the American Society for Reproductive Medicine/Society
for Assisted Reproductive Technology Registry. Fertil. Steril., 77, 18-31.
Seppala, M., Rutanen, E.M., Jalanko, H., Lehtovirta, P., Stenman, U.H. and
Engvall, E. (1978) Pregnancy-specific beta 1-glycoprotein and chorionic
gonadotropin-like immunoreactivity during the latter half of the cycle in women
using intrauterine contraception. J. Clin. Endocrinol. Metab., 47, 1216-1219.
Sharp, N.C., Anthony, F., Miller J.F. and Masson G.M. (1986) Early conceptual
loss in subfertile patients. Br. J. Obstet. Gynaecol., 93, 1072- 1077.
Shutt, D.A. and Lopata, A. (1981) The secretion of hormones during the culture
of human preimplantation embryos with corona cells. Fertil. Steril., 35, 413^16.
Simon, C., Garcia-Velasco, J.A., Valbuena, D., Peinado, J.Α., Moreno, C., Remohi,
J. and Pellicer, A. (1998) Increased uterine receptivity by decreasing estradiol
levels during the preimplantation period in high responder patients by using an
FSH step-down regimen. Fertil. Steril., 70, 234-239.
Simon, C., Landeras, J., Zuzuarregui J.L., Martin, J.C., Remohi, J. and Pellicer,
A. (1999) Early pregnancy losses in in vitro fertilization and oocyte donation.
Fertil. Steril., 72, 1061-1065.
Sinosich, M.J., Grudzinskas, J.G. and Saunders, D.M. (1985) Placental proteins
in the diagnosis and evaluation of the 'elusive' early pregnancy. Obstet.
Gynecol. Surv., 40, 273-282.
Slama, R., Eustache, F., Ducot, B., Jensen, T.K., J0rgensen N., Horte, Α.,
Irvine, S., Suominen, J., Anderson, A.G., Auger, J. et al. (2002) Time to
pregnancy and semen parameters: a cross-sectional study among fertile couples
from four European cities. Hum. Reprod., 17, 503-515.
Snijders, A.M., Nowak, N., Segraves, R., Blackwood, S., Brown, N., Conroy, J.,
Hamilton, G., Hindle, A.K., Huey, B., Kimura, K. et al. (2001) Assembly of
microarrays for genome-wide measurement of DNA copy number. Nature Genet., 29,
263-264
Stewart, D.R., Overstreet, J.W., Celniker, A.C., Hess, D.L., Cragun, J.R.,
Boyers, S.P. and Lasley, B.L. (1993) The relationship between hCG and relaxin
secretion in normal pregnancies vs. peri-implantation spontaneous abortions.
Clin. Endocrinol. (Oxf.), 38, 379-385.
Tamsen, L. and Eneroth, P. (1986) Serum levels of pregnancy-specific beta 1-
glycoprotein (SP1) and human chorionic gonadotropin (beta-hCG) in women using an
intrauterine device. Contraception, 33, 497-501
Templeton, Α., Morris, J.K. and Parslow, W. (1996) Factors that affect outcome
of in-vitro fertilisation treatment. Lancet, 348, 1402-1406.
Tur-Kaspa, I., Confino, E., Dudkiezicz, A.B., Myers, S.A., Friberg, J, and
Gleicher, N. (1990) Ovarian stimulation protocol for in-vitro fertilization with
gonadotropin-releasing hormone agonist widens the implantation window. Fertil.
Steril., 53, 859-864.
Vaitukaitis, J.L., Braunstein, G.D. and Ross, G.T. (1972) A radioimmunoassay
which specifically measures human chorionic gonadotropin in the presence of
luteinizing hormone. Am. J. Obstet. Gynecol., 113, 751-758.
van Noord-Zaadstra, B.M., Looman, C.W., Alsbach, H., Habbema, J.D., te Velde,
E.R. and Karbaat, J. (1991) Delaying childbearing: effect of age on fecundity
and outcome of pregnancy. Br. Med. J., 302, 1361-1365.
Vegetti, W., Van Assche, E., Frias, Α., Verheyen, G., Bianchi, M.M., Bonduelle,
M., Liebaers, I. and Van Steirteghem, A. (2000) Correlation between semen
parameters and sperm aneuploidy rates investigated by fluorescence in-situ
hybridization in infertile men. Hum. Reprod., 15, 351-365.
Verlinsky, Y. and Evsikov, S. (1999) Karyotyping of human oocytes by chromosomal
analysis of the second polar bodies. Mol. Hum. Reprod., 5, 89-95.
Vidal, F., Rubio, C., Simon, C., Gimenez, C., Minguez, Y., Pellicer, Α., Santalo,
J., Remohi, J. and Egozcue J. (2000) Is there a place for preimplantation
genetic diagnosis screening in recurrent miscarriage patients? J. Reprod. Fertil.,
55 (Suppl.), 143-146.
Voullaire, L., Slater, H., Williamson, R. and Wilton, L. (2000) Chromosome
analysis of blatomeres from human embryos by using comparative genomic
hybridization. Hum. Gen., 106, 210-217.
Walker, E.M., Lewis, M., Cooper, W., Marnie, M. and Howie, P.W. (1988) Occult
biochemical pregnancy: fact or fiction? Br. J. Obstet. Gynaecol., 95, 659-663.
Wehmann, R.E., Ayala, A.R., Birken, S., Canfield, R.E. and Nisula, B.C. (1981)
Improved monitoring of gestational trophoblastic neoplasia using a highly
sensitive assay for urinary human chorionic gonadotropin. Am. J. Obstet.
Gynecol., 140, 753-757.
Wells, D. and Delhanty, J.D.A. (2000) Comprehensive chromosomal analysis of
human preimplantation embryos using whole genome amplification and single cell
comparative genome hybridization. Mol. Hum. Reprod., 6, 1055-1062.
White, R.F., Hertig, A.T., Rock, J. and Adams, E.C. (1951) Histological and
histochemical observations on the corpus lutea associated with early normal and
abnormal ova. Contrib. Embryol. Carneg. Inst., 34, 55-74.
Whittaker, P.G., Taylor, A. and Lind, T. (1983) Unsuspected pregnancy loss in
healthy women. Lancet, i, 1126-1127.
Wilcox, A.J., Weinberg, C.R., Wehmann, R.E., Armstrong E.G., Canfield, R.E. and
Nisula, B.C. (1985) Measuring early pregnancy loss: laboratory and field
methods. Fertil. Steril., 44, 366-374.
Wilcox, A.J., Weinberg, C.R., O'Connor, J.F., Baird, D.D., Schlatterer, J.P,
Canfield, R.E., Armstrong, E.G. and Nisula, B.C. (1988) Incidence of early loss
of pregnancy. N. Engl. J. Med., 319, 189-194.
Wilcox, A.J., Baird, D.D. and Weinberg, C.R. (1999) Time of implantation of the
conceptus and loss of pregnancy. N. Engl. J. Med., 340, 1796-1769.
Wilton, L., Williamson, R., McBain, J., Edgar, D. and Voullaire, L. (2001) Birth
of a healthy infant after preimplantation confirmation of euploidy by
comparative genomic hybridization. N. Engl. J. Med., 345, 1537-1541.
Wolkersdorfer, G.W., Bornstein, S.R., Hibers, U., Zimmermann, G., Bieslod, S.,
Lehmann, M. and Alexander, H. (1998) The presence of chorionic gonadotrophin β
subunit in normal cyclic human endometrium. Mol. Hum. Reprod., 4, 179-184.
Wright Bates, G. and Ginsburg, E.S. (2002) Early pregnancy loss in in vitro
fertilization (IVF) is a postive predictor of subsequent IVF success. Fertil.
Steril., 11, 337-341.
Yovich, J.L., Wilcox, D.L., Girudzinskao, J.G. and Bolton, A.E. (1986) The
prognostic value of hCG, PAPP-A, E2 and Ρ in the early human pregnancy. Aust. NZ
J. Obstet. Gynaecol., 26, 59-65.
Zinamen, M.J., Clegg, E.D., Brown, C.C., O'Connor, J. and Seleven, S.G. (1996)
Estimates of human fertility and pregnancy loss. Fertil. Steril., 65, 503-509.
Δείτε Επίσης
Αυτόματες , Πρώϊμες , Και Κρυφές Αποβολές
Θρομβοφιλία (κληρονομική ή και επίκτητη)
Μετάλλαξη Προθρομβίνης FII G20210A
Plasminogen Activator Inhibitor - 1 : Αναστολέας του Ενεργοποιητή του Ιστικού Πλασμινογόνου - 1
Η σελίδα έχει εώς τώρα
Επισκέπτες
